En thermodynamique, on emploie souvent les termes « isotherme » et « monotherme », afin de décrire une transformation, cependant ces deux expressions n’ont pas la même signification !
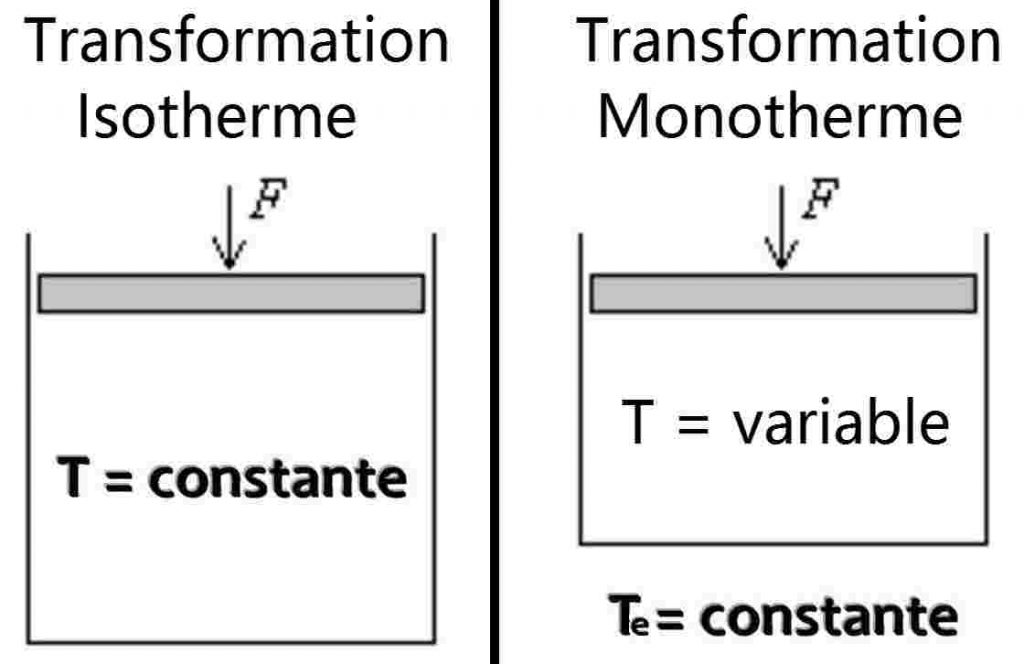
En effet, un phénomène isotherme renvoie à une transformation (physique ou chimique) au cours de laquelle la température du système est constante.
Tandis qu’un phénomène monotherme renvoie à une transformation qui s’effectue dans un système où le milieu extérieur est à température constante.
Le préfixe iso- peut aussi s’appliquer à la pression (isobare), ou encore au volume du système (isochore).
Le préfixe mono- peut aussi s’appliquer à la pression (monobare).
Astuce :
Pour ne plus confondre les préfixes iso- et mono- , l’astuce consiste à se dire que :
Dans système, on a le même s que dans iso- , ainsi une transformation iso- est caractéristique du système.
A l’inverse, dans milieu extérieur, on le même m que dans mono- , ainsi une transformation mono- est caractéristique du milieu extérieur.
- Les trois singes de la sagesse : Mizaru, Kikazaru, Iwazaru - 18 décembre 2025
- Pâte brisée, sablée ou feuilletée ? - 11 décembre 2025
- Différence entre poulpe, pieuvre et calamar - 18 mars 2025
Rejoignez-nous sur Instagram !
Découvrez nos infographies et astuces : @JeRetiensNet


merci pour la clarification meme si 6ans a passé.
:)
Merci beaucoup! Maintenant je suis sûre de ne plus me tromper ;)
Je suis tombée sur la publication Facebook, j’étais très intriguée par l’accroche et je ne suis pas déçue ! Je vais peut-être devenir une adepte… ;-)