Les réactions organiques sont classées en fonction de leur équation bilan et de leur mécanisme. Il existe 3 réactions organiques fondamentales : réaction d’addition, d’élimination, et de substitution. Cet article s’intéresse uniquement à cette dernière réaction organique : la réaction de substitution nucléophile (d’ordre 1 et 2) !
– La substitution nucléophile d’ordre 1 (SN1) :
La SN1 se déroule en deux étapes, lorsque la molécule de départ est très encombrée :
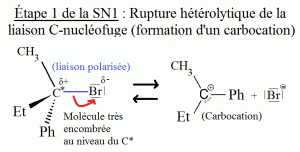
Étape 1 : Rupture hétérolytique de la liaison C-nucléofuge (formation d’un carbocation).
Une rupture hétérolytique est une rupture d’une liaison covalente dans une molécule neutre générant un anion et un cation.
Les groupes d’atomes qui vont être présents dans la réaction de substitution nucléophile d’ordre 1 (SN1), et plus particulièrement autour du carbone asymétrique (C*) sont : l’atome de Brome (Br), le groupe méthyle (CH3), le groupe éthyle (Et ou C2H5), le groupe phényle (Ph ou C6H5) qui est un cycle, ainsi qu’un groupe fonctionnel aromatique. Ce sont donc des grosses molécules, qui favorisent l’encombrement du Carbone asymétrique (C*).
Lorsque la molécule (en représentation de Cram) est très encombrée, une rupture hétérolytique (rupture dissymétrique d’une liaison covalente) de la liaison C-nucléofuge (C-Br) peut se produire, dû au fait qu’elle soit plus polarisée que les autres et que le carbone asymétrique soit encombré. Cette rupture hétérolytique forme alors deux ions de charges différentes, dans notre exemple ci-dessus, il s’agit de l’ion Bromure (Br-) et du Carbocation (C+) (un carbocation est un ion dérivé d’un composé organique, qui possède une charge électrique positive sur un ou plusieurs atomes de carbone, ainsi qu’une lacune électronique représentée par le rectangle en-dessous du Carbone (C+) ; les carbocations sont des intermédiaires de réaction). Cette lacune électronique confère alors à cet atome de carbone des propriétés électrophiles qui vont permettre la deuxième étape.
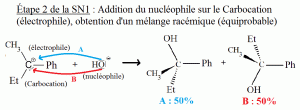
Étape 2 : Addition du nucléophile sur le carbocation (C+).
Dans la deuxième étape de la SN1, l’ion hydroxyde (OH-) est un nucléophile (espèce chimique qui aime les noyaux, donc qui aime les charges positives) cède un doublet d’électrons au carbone électrophile (qui aime les électrons, donc les charges négatives) ; ce mécanisme induit une racémisation (transformation d’un énantiomère pur en mélange racémique (mélange des deux énantiomères en quantités égales, soit 50%) d’un composé chiral), en effet l’attaque du nucléophile se fait de manière équiprobable des 2 côtés du plan du Carbocation (C+), on obtient alors soit le composé A soit le composé B, selon l’angle d’attaque du nucléophile sur l’électrophile.
La première étape de la SN1 est difficile, tandis que la deuxième est facile, donc l’étape 1 est cinétiquement déterminante (ECD), c’est l’étape 1 qui met le plus de temps à être réalisée. La vitesse de la SN1 est donc : V(sn1) = V1 = k[X] avec k une constante de vitesse et [X] la concentration d’un composé X (dans l’exemple ci-dessus, le composé X correspond à la toute première molécule de l’étape 1). La vitesse de réaction, ainsi que le temps nécessaire pour qu’elle se réalise sont des informations primordiales au niveau industriel, c’est pourquoi il est intéressant de les connaître.
– La substitution nucléophile d’ordre 2 (SN2) :
La SN2 se déroule en une seule étape bimoléculaire (2 molécules différentes réagissent entre elles), lorsque la molécule de départ est peu encombrée.
Les groupes d’atomes qui vont être présents dans la réaction, et plus particulièrement autour du carbone asymétrique (C*) sont : l’atome de Brome (Br), le groupe méthyle (CH3), l’Hydrogène (H), le Deutérium (D) (qui est un isotope naturel de l’hydrogène, c’est-à-dire que ce sont deux atomes possédant le même nombre d’électrons), le Deutérium est utilisé ici pour que la molécule soit en représentation de Cram (c’est-à-dire avec une carbone asymétrique C*, sinon il ne serait pas possible d’avoir une substitution nucléophile). Ce sont donc des groupes d’atomes peu encombrants, grâce auxquels la gène stérique (ou encombrement stétique) est minimale.
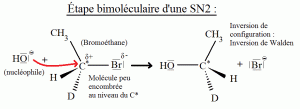
Dans la SN2, le nucléophile (espèce chimique qui aime les noyaux, donc qui aime les charges positives) attaque du côté opposé au nucléofuge (aussi appelé groupe partant, qui est une espèce chimique ayant la capacité de se détacher d’une molécule), ce qui produit une inversion de configuration au niveau du carbone asymétrique (C*), qu’on appelle « Inversion de Walden ».
Ainsi, dans l’exemple ci-dessous, le nucléophile (HO-) attaque du côté opposé au nucléofuge (Br), ce qui produit une inversion de Walden.
Puisque la SN2 se réalise en une seule étape, contrairement à la SN1, la vitesse de la SN2 est donc : V(sn2) = k[X][Y] avec k une constante de vitesse et [X], [Y] les concentrations respectives des composés X et Y (dans l’exemple ci-dessus, le composé X correspond au Bromoéthane, et le composé Y correspond à l’ion hydroxyde (HO-).
Astuces :
Pour se souvenir que la SN1 a lieu lorsque la molécule est encombrée (lorsque la gène stérique est élevée), il faut penser au mot « plein » comme « 1 », tandis que pour la SN2 qui est moins (peu) encombrée (avec une gène stérique faible), il faut penser au mot « peu » comme 2 !
Pour se souvenir des vitesses, il suffit de retenir le nombre de lettres : une lettre pour la SN1 (V(sn1) = V1 = k[X]) et deux lettres pour la SN2 (V(sn2) = k[X][Y]) !
Enfin, pour se souvenir que l’inversion de Walden est spécifique à une SN2, il faut se dire que le « W » de Walden est composé de 2 « V » !
- Les trois singes de la sagesse : Mizaru, Kikazaru, Iwazaru - 18 décembre 2025
- Pâte brisée, sablée ou feuilletée ? - 11 décembre 2025
- Différence entre poulpe, pieuvre et calamar - 18 mars 2025
Rejoignez-nous sur Instagram !
Découvrez nos infographies et astuces : @JeRetiensNet


Un grand merci pour ces explications clairs et completes…. signé un prof de collège
merci beaucoup pour vos explications,mais j’aimerais savoir svp est-ce qu’une SN1 se fait toujours avec racemisation?
Merci pour vos explications, sa nous aident à comprendre comment on doit
traiter un exercice
Merci beaucoup