De nombreuses réactions chimiques et biologiques se produisent continuellement à l’intérieur et à l’extérieur du corps humain. Certaines d’entre elles sont spontanées et d’autres ne sont pas spontanées. Les réactions spontanées sont appelées réactions exergoniques alors que les réactions non spontanées sont appelées réactions endergoniques.
Réactions endergoniques
Définition de la réaction endergonique
Une réaction endergonique est une réaction chimique qui nécessite un apport d’énergie pour se réaliser.
Endergonique vient du grec endo– (ἔνδον) qui veut dire dedans et ergo– (ἔργον) qui veut dire travail.
Cette étymologie permet de comprendre le concept: il s’agit d’une réaction qui nécessite l’aide d’un travail (donc de l’apport d’une énergie).
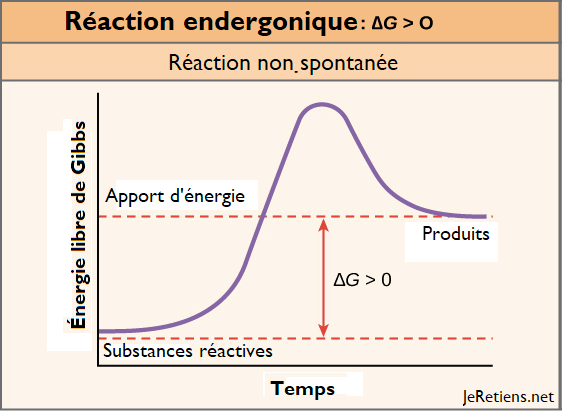
Fonctionnement d’une réaction endergonique
Il y a de nombreuses réactions dans la nature qui ne peuvent se produire que lorsqu’une quantité suffisante d’énergie provenant de l’environnement est fournie. A elles seules, ces réactions ne peuvent pas se produire car elles nécessitent une grande quantité d’énergie pour briser les liaisons chimiques.
L’énergie externe aide à briser ces liens. L’énergie libérée par la rupture des liaisons maintient alors la réaction en marche. Parfois, l’énergie libérée lors de la rupture des liaisons chimiques est trop faible pour soutenir la réaction. Dans ce cas, une énergie externe est nécessaire pour que la réaction se poursuive. De telles réactions sont appelées réactions endergoniques.
Dans la thermodynamique chimique, ces réactions sont également appelées réactions défavorables ou non spontanées. L’énergie libre de Gibbs est positive à température et pression constantes, ce qui signifie que plus d’énergie est absorbée plutôt que libérée.
Exemples de réactions endergoniques
Des exemples de réactions endergoniques comprennent la synthèse protéique, la pompe sodium – potassium sur la membrane cellulaire, la conduction nerveuse et la contraction musculaire ou encore la photosynthèse chez les plantes.
- La synthèse des protéines est une réaction anabolique qui exige que de petites molécules d’acides aminés se rassemblent pour former une molécule de protéine. Elle implique beaucoup d’énergie pour former les liaisons peptidiques.
- La pompe à potassium sodique sur la membrane cellulaire s’occupe du pompage des ions sodium et du mouvement des ions potassium contre le gradient de concentration pour permettre la dépolarisation cellulaire et la conduction nerveuse. Ce mouvement contre le gradient de concentration nécessite beaucoup d’énergie qui provient de la dégradation de la molécule d’adénosine triphosphate (ATP).
- La contraction musculaire ne peut se produire que lorsque les liaisons existantes entre l’actine et les fibres de myosine (protéines musculaires) se rompent pour former de nouvelles liaisons. Cela nécessite également une quantité énorme d’énergie qui provient de la décomposition de l’ATP. C’est pour cette raison que l’ATP est connue sous le nom de molécule d’énergie universelle.
- La photosynthèse chez les plantes est un autre exemple de réaction endergonique. La feuille contient de l’eau et du glucose, mais elle ne peut pas produire sa propre nourriture si elle n’est pas exposée au soleil. Dans ce cas, la lumière du soleil est la source d’énergie externe.
- La fonte de la glace nécessite une chaleur latente pour atteindre le point de fusion. Le processus pour atteindre le niveau de barrière d’énergie d’activation de l’état de transition est endergonique. Une fois l’étape de transition atteinte, la réaction peut se poursuivre et la fonte continuer.
Réactions exergoniques
Définition de la réaction exergonique
Une réaction exergonique est une réaction chimique spontanée dont le travail est fourni durant sa propre réalisation sans apport énergétique extérieur.
Exergonique vient du grec exo- (ἔξω) qui veut dire hors de et ergo- (ἔργον) qui veut dire travail.
Cette étymologie permet de comprendre le concept: il s’agit d’une réaction qui se déroule sans qu’on lui fournisse du travail (de l’énergie), sous une autre forme que de la chaleur. Cependant, la réaction exergonique peut produire de la chaleur (ex: fonctionnement d’une pile).
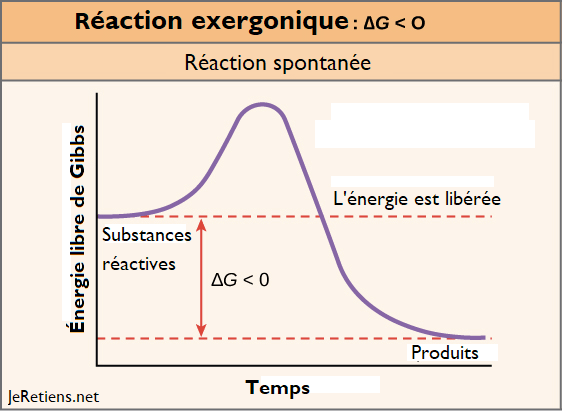
Fonctionnement de la réaction exergonique
Ces réactions sont des réactions irréversibles qui surviennent spontanément dans la nature.
Par spontané, cela signifie que la réaction se produit avec très peu de stimuli externes.
Par exemple, la combustion du sodium lorsqu’il est exposé à l’oxygène présent dans l’atmosphère. La combustion d’une bûche est un autre exemple de réactions exergoniques.
De telles réactions libèrent plus de chaleur et sont appelées réactions favorables dans le domaine de la thermodynamique chimique.
L’énergie libre de Gibbs est négative à température et pression constantes, ce qui signifie que plus d’énergie est libérée plutôt qu‘absorbée. Ce sont des réactions irréversibles.
Exemples de réactions exergoniques
Comme nous l’avons exposé ci-dessus, de nombreux exemples de réactions exergoniques concernent la combustion (au contact de l’oxygène, par exemple), en voici quelques autres comme la respiration cellulaire ou les réactions cataboliques de décomposition.
- La respiration cellulaire est un exemple classique de réaction exergonique. Environ 3012 kJ d’énergie sont libérés lorsqu’une molécule de glucose est convertie en dioxyde de carbone. Cette énergie est utilisée par les organismes pour d’autres activités cellulaires.
- Toutes les réactions cataboliques, c’est-à-dire la décomposition d’une grosse molécule en molécules plus petites, sont des réactions exergoniques.
Par exemple, la décomposition des glucides, des lipides et des protéines a libéré de l’énergie pour que les organismes vivants puissent faire leur travail.
Réactions exergoniques à apport énergétique extérieur
Certaines réactions exergoniques ne se produisent pas spontanément et nécessitent un petit apport d’énergie pour déclencher la réaction. Cet apport d’énergie est appelé énergie d’activation. Une fois que le besoin en énergie d’activation est satisfait par une source extérieure, la réaction se rompt et forme de nouvelles liaisons et l’énergie est libérée au fur et à mesure que la réaction se déroule. Il en résulte un gain net d’énergie dans le système environnant et une perte nette d’énergie dans le système de réaction.
- Comment gagner aux jeux de hasard : comprendre les mécanismes du hasard et de la stratégie - 28 octobre 2025
- Mathématiques de la roulette et du poker - 19 septembre 2025
- Comprendre Emmanuel Kant - 13 mai 2025
Rejoignez-nous sur Instagram !
Découvrez nos infographies et astuces : @JeRetiensNet


c’est super
J’ai vraiment aimé, ça m’a aidé à différencier les différents lots qui même en lisant dans le dictionnaire je ne comprenais pas mais cette page éclaircit bien les mots et donne des exemples très compréhensifs, vraiment j’ai aimé.
La germination est elle un processus endorgonique?